‘आवर्त सारणी’ PDF Quick download link is given at the bottom of this article. You can see the PDF demo, size of the PDF, page numbers, and direct download Free PDF of ‘Periodic Table In Hindi’ using the download button.
118 Elements Name List PDF And Periodic Table In Hindi PDF Free Download
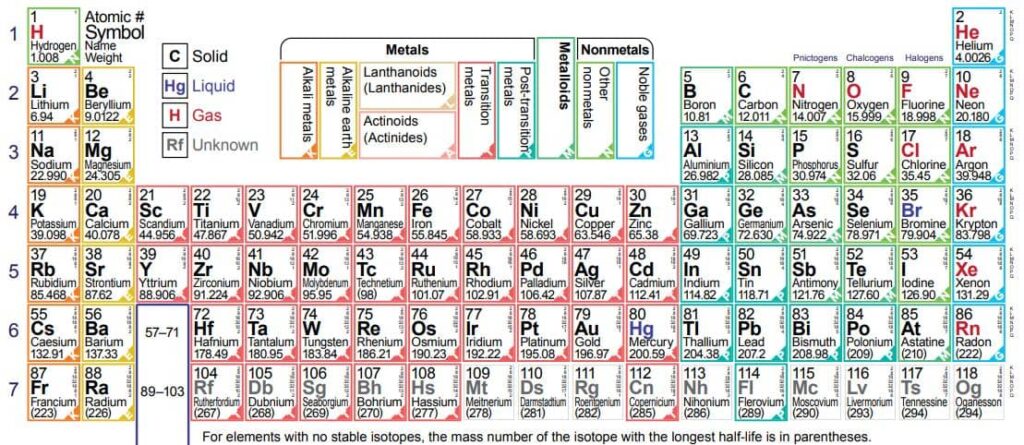
आवर्त सारणी इन हिंदी
Periodic Table आवर्त सारणी : जिसको मेण्डलीफ का आवर्त नियम भी कहते है, मेण्डलीफ की मूल आवर्त सारणी के मुख्य लक्षण, आधुनिक आवर्त नियम, Medal’s का नियम इस लेख के माध्यम से हम आपको आवर्त सारणी (Periodic Table) के बारे में जानकारी देंगे तथा नीचे हमने Periodic Table PDF Format में भी प्रस्तुत कि हुई है, आप उसे भी Free Download Period Table कर सकते है।
मेण्डलीफ की लघु रूप आवर्त सारणी के दोष, दीर्घाकार आवर्त सारणी (Long Form Periodic Table) आदि से सम्बन्धित प्रश्नो की जानकारी के लिए हमारे इस लेख को ध्यान से पढ़े और इन्हे याद करलें क्यों की यहाँ से कई बार प्रश्नों को पूछ लिया जाता है।
बहुत समय पहले से वैज्ञानिक तत्वों को एक क्रमबध्द और सरल रूप में व्यवस्थित करने का प्रयास करते रहे थे। इस दिशा में डॉबेराइनर (1817), जे. ए. आर. न्यूलैण्ड (1864), ड़ी. आई. मेन्डेलीफ (1869) और लोथर मेयर (1870) के योगदान अत्यंत महत्वपूर्ण साबित हुए।
तत्वों का प्रथम आवर्ती वर्गीकरण रशियन वैज्ञानिक मेन्डेलीफ की देन है। आधुनिक आवर्त सारणी मेन्ड्रेलीफ द्वारा प्रस्तुत आवर्त सारणी का ही आधुनिक रूप है।
सर्वप्रथम तत्वों को धातु और अधातु दो वर्गों में बाँटा गया, धातु वे होते है। जिनमें निम्नलिखित गुण होतें हैं
याद रखने के लिए आप इस pdf को print करवाके दीवाल पर चिपका दे उसको हररोज पढ़े, धीरज के साथ याद रखने की कोशिश करे। 118 नाम को आप 30 -30 के चार भागो में बाँटकर याद रखे।
मुख्य विशेषताएं:
- वर्ग – आवर्त सारणी में 18 ऊर्ध्वाधर स्तंभ (Vertical Columns) होते हैं। प्रत्येक स्तंभ एक वर्ग कहलाता है। एक वर्ग के सभी तत्वों के समान रासायनिक और भौतिक गुण-धर्म होते हैं क्योंकि उनके बाहरी इलेक्ट्रॉनों की संख्या समान होती है।
- आवर्त – आवर्त सारणी में तत्व पंक्तियों में क्रमबद्ध होते हैं। समान आवर्त के तत्वों की इलेक्ट्रॉन कक्षाओं की संख्या समान होती है।
संबंधित शब्दावलियां:
तत्वों का वर्गीकरण:
- वर्ग 1 में, जिसका स्थान सबसे बाईं ओर होता है, उसमें क्षारीय धातु रहते हैं (Li, Na, K, Rb, Cs और Fr)।
- क्षारीय मृदा धातु वे धात्विक तत्व होते हैं जो आवर्त सारणी के वर्ग 2 में पाए जाते हैं।
- आवर्त सारणी के मध्य भाग में वर्ग 3 -12 में पाए जाने वाले तत्व संक्रमण तत्व कहलाते हैं। संक्रमण तत्वों में, संयोजी इलेक्ट्रॉन एक से अधिक शेल में मौजूद होते हैं। कुछ मामूली अपवाद के साथ, संक्रमण धातु परमाणुओं की इलेक्ट्रॉनिक संरचना को [ns2 (n-1)d]m के रूप में लिखा जा सकता है, जहां आंतरिक d कक्षा में संयोजी-शेल s कक्षा की तुलना में अधिक ऊर्जा होती है।
- वर्ग 18 में, जो कोष्टक सबसे दाईं ओर होता है, आदर्श गैसें होती हैं ( He, Ne, Ar, Kr, Xe और Rn )। उनके सबसे बाहरी शेल्स में 8 इलेक्ट्रॉन होते हैं, He को छोड़कर, क्योंकि इसका बाहरी शेल होता है K और इसमें अधिकतम 2 इलेक्ट्रॉन ही रह सकते हैं।
- आंतरिक संक्रमण तत्व:
- परमाणु संख्या 58 से 71 (Ce से Lu) वाले 14 तत्व लैंथेनाइड्स कहलाते हैं और उन्हें तत्व लैंथेनम (La), समान अवस्थिति (आवर्त 6 में वर्ग 3) में परमाणु संख्या 57, के साथ रखा जाता है क्योंकि उनके बीच बहुत अधिक समानता है। हालांकि, सुविधा के लिए, उन्हें मुख्य आवर्त सारणी के नीचे अलग से दिखाया जाया है।
- परमाणु संख्या 90 से 103 (Th से Lr) वाले 14 तत्व ऐक्टिनाइड्स कहलाते हैं और उन्हें तत्व लैंथेनम (Ac), समान अवस्थिति (आवर्त 7 में वर्ग 3) में परमाणु संख्या 89, के साथ रखा जाता है क्योंकि उनके बीच बहुत अधिक समानता है। उन्हें भी मुख्य आवर्त सारणी के नीचे लैंथेनाइड्स के साथ दिखाया जाता है।
आधुनिक आवर्त सारणी हिंदी में
| परमाणु संख्या | नाम एवं संकेत | परमाणु भार | खोजकर्ता | वर्ष |
|---|---|---|---|---|
| 1 | हाइड्रोजन (H) | 1.0079 | एच. कैवेन्डिश | 1766 |
| 2 | हीलियम (He) | 4.0026 | पी. जानस्सेन व एन. लॉकएर | 1868 |
| 3 | लीथियम (Li) | 6.941 | जे.ए. अर्फवेडसन | 1817 |
| 4 | बेरेलियम (Be) | 9.0122 | एल.एन. वाऊक्वेलिन | 1798 |
| 5 | बोरॉन (B) | 10.811 | जे. एल. लुजेक, एल. जे. थेनार्ड, एच. डेवी | 1808 |
| 6 | कार्बन (C) | 12.0107 | अज्ञात | 3750 ईसा-पूर्व |
| 7 | नाइट्रोजन (N) | 14.0067 | डी. रदरफोर्ड | 1772 |
| 8 | ऑक्सीजन (O) | 15.994 | शीले एवं प्रीस्टले | 1772 |
| 9 | फ्लोरीन (F) | 18.9984 | एच. मोइसन | 1886 |
| 10 | नियॉन (Ne) | 20.1797 | डब्ल्यू. रामसे व एम. ट्रेवर्स | 1898 |
| 11 | सोडियम (Na) | 22.9897 | एच. डेवी | 1807 |
| 12 | मैग्नीशियम (Mg) | 24.305 | जे. ब्लैक | 1755 |
| 13 | अल्युमिनियम (Al) | 26.9815 | एच. सी. ओर्स्टेड | 1825 |
| 14 | सिलिकॉन (Si) | 28.0855 | जे. बर्जेलियम | 1823 |
| 15 | फॉस्फोरस (p) | 30.9738 | एच. ब्रांड | 1669 |
| 16 | सल्फर (S) | 32.065 | अज्ञात | – |
| 17 | क्लोरीन (Cl) | 35.453 | के. शीले | 1774 |
| 18 | ऑर्गन (Ar) | 39.948 | डब्ल्यू रामसे व जे. रेले | 1894 |
| 19 | पोटैशियम (k) | 39.0983 | एच. डेवी | 1807 |
| 20 | कैल्सियम (Ca) | 40.078 | एच. डेवी | 1808 |
| 21 | स्कैण्डियम (Sc) | 44.9559 | एल.एफ.निल्सन | 1879 |
| 22 | टाइटेनियम (Ti) | 47.867 | डब्ल्यू. ग्रेगर | 1791 |
| 23 | वनेडियम (V) | 50.9415 | ए.एम.डी.रियो | 1801 |
| 24 | क्रोमियम (Cr) | 51.9961 | एल.एन. वाऊक्वेलिन | 1797 |
| 25 | मैंगनीज़ (Mn) | 54.938 | जे.जी. गन एवं आई. जी. कैम | 1774 |
| 26 | आइरन (Fe) | 55.845 | अज्ञात | – |
| 27 | कोबाल्ट (Co) | 58.9332 | जी. ब्रांट | 1735 |
| 28 | निकल (Ni) | 58.6934 | ए. क्रॉन्सटेड्ट | 1751 |
| 29 | कॉपर (Cu) | 63.546 | अज्ञात | – |
| 30 | जिंक (Zn) | 65.39 | अज्ञात | – |
| 31 | गैलियम (Ga) | 69.723 | डि. ब्यासबाऊड्रेन | 1875 |
| 32 | जर्मेनियम (Ge) | 72.64 | सी. विंकलर | 1886 |
| 33 | आर्सेनिक (As) | 74.9216 | ए. मैग्नेस | 2500 ईसा-पूर्व |
| 34 | सेलेनियम (Se) | 78.96 | जे. बर्जेलियम | 1817 |
| 35 | ब्रोमीन (Br) | 79.904 | ए.जे. बालार्ड एवं सी.जे. लोविग | 1826 |
| 36 | क्रिप्टॉन (Kr) | 83.8 | डब्ल्यू रामसे व एम. ट्रेवर्स | 1898 |
| 37 | रुबिडियम (Rb) | 85.4678 | आर. बुनसेन व जी. किरचॉफ | 1861 |
| 38 | स्ट्रोन्शियम (Sr) | 87.62 | डब्ल्यू क्रुकशंक | 1790 |
| 39 | वाईटरियम (Y) | 88.9059 | जे. गेबोलिन | 1794 |
| 40 | ज़र्कोनियम (Zr) | 91.224 | एम.एच. क्लापोर्थ | 1789 |
| 41 | नायोबियम (Nb) | 92.9064 | सी. हैचेट | 1801 |
| 42 | मॉलीब्डेनम (Mo) | 95.94 | के. शीले | 1778 |
| 43 | टेक्निशियम (Tc) | 98 | ए. जे.सेगर व सी. पेरियर | 1937 |
| 44 | रूथेनियम (Ru) | 101.07 | के. क्लाउस | 1844 |
| 45 | रोह्डियम (Rh) | 102.9055 | डब्ल्यू वोलेस्टीन | 1803 |
| 46 | पैलेडियम (Pd) | 106.42 | डब्ल्यू. वोलेस्टीन | 1803 |
| 47 | सिल्वर (Ag) | 107.8682 | अज्ञात | – |
| 48 | कैडमियम (Cd) | 112.411 | एफ. स्ट्रोमेएर एवं के.एस.हर्मन | 1817 |
| 49 | इण्डियम (In) | 114.818 | एफ. रीच व टी. रिक्टर | 1863 |
| 50 | टिन (Sn) | 118.71 | अज्ञात | – |
| 51 | ऐन्टिमोनी (Sb) | 121.76 | अज्ञात | 3000 ईसा-पूर्व |
| 52 | टेल्यूरियम (Te) | 127.6 | एम. वॉन रीचेन्स्टीन | 1782 |
| 53 | आयोडीन (I) | 126.9045 | बी. कर्टियस | 1811 |
| 54 | जेनॉन (Xe) | 131.293 | डब्ल्यू. रामसे व एम. ट्रेवर्स | 1898 |
| 55 | सीज़ियम (Cs) | 132.9055 | आर. बुनसेन, जी. किरचौफ | 1860 |
| 56 | बेरियम (Ba) | 137.327 | शीले एवं डेवी | 1808 |
| 57 | लैन्थेनम (La) | 138.9055 | सी. मोसान्देर | 1839 |
| 58 | सीरियम (Ce) | 140.116 | जे. बर्जेलियस व डब्ल्यू हिस्लिंगर | 1803 |
| 59 | प्रसियोडाइमियम (Pr) | 140.9077 | सी. वॉन वेल्सबाख | 1885 |
| 60 | नियोडाइमियम (Nd) | 144.24 | सी. वॉन वेल्सबाख | 1885 |
| 61 | प्रोमेथियम (Pm) | 145 | जे. मरिन्सकी | 1945 |
| 62 | समेरियम (Sm) | 150.36 | एल डि ब्यासबाऊड्रेन | 1879 |
| 63 | युरोपियम (Eu) | 151.964 | एच. डिमैके | 1901 |
| 64 | गेडोलिनियम (Gd) | 157.25 | डि. मैरिग्नैक | 1880 |
| 65 | टर्बियम (Tb) | 158.9253 | सी. मोसेन्डर | 1843 |
| 66 | डिसप्रोसियम (Dy) | 162.5 | एल डी ब्यासबाऊड्रेन | 1886 |
| 67 | होल्मियम (Ho) | 164.9303 | जे. सोरेट व एम. डेलाफोन्टेई | 1878 |
| 68 | इरबियम (Er) | 167.259 | सी. मोसेन्डर | 1839 |
| 69 | थुलियम (Tm) | 168.9342 | पी. क्लीव | 1879 |
| 70 | वाईटर्बियम (Yb) | 173.04 | सी. मैरिग्नैक | 1878 |
| 71 | लुटीशियम (Lu) | 174.967 | जी. अर्बेन | 1907 |
| 72 | हाफ्नियम (HF) | 178.49 | डी. कॉस्टर एवं डि. हेवेसी | 1923 |
| 73 | टेन्टेलम (Ta) | 180.9479 | ए. इकेबर्ग | 1802 |
| 74 | टंगस्टन (W) | 183.84 | जॉन जोश एवं फोस्टो एल्युअर | 1783 |
| 75 | रीनियम (Re) | 186.207 | डब्लु. नोड्डाक व अन्य | 1925 |
| 76 | ओस्मियम (Os) | 190.23 | एस. टेनेंट | 1803 |
| 77 | इरीडियम (Ir) | 192.217 | एस. टेनेंट | 1803 |
| 78 | प्लैटिनम (pt) | 195.078 | ए.डि. उल्लोआ | 1735 |
| 79 | गोल्ड (Au) | 196.9665 | अज्ञात | – |
| 80 | मरकरी (Hg) | 200.59 | अज्ञात | – |
| 81 | थैलियम (Ti) | 204.3833 | डब्ल्यू. क्रूक्स | 1861 |
| 82 | लेड (Pb) | 207.2 | अज्ञात | – |
| 83 | बिस्मथ (Bi) | 208.9804 | जी. एग्रीकोला | 1953 |
| 84 | पोलोनियम (Po) | 209 | पियरे व मैडम क्यूरी | 1898 |
| 85 | एस्टेटाइन (At) | 210 | डी.आर.मैकेंजी एवं के.आर. मैकेंजी | 1940 |
| 86 | रेडॉन (Rn) | 222 | फ्रेडरिक अर्नेस्ट | 1900 |
| 87 | फ्रैंसियम (Fr) | 223 | एम. पेरे | 1939 |
| 88 | रेडियम (Ra) | 226 | पियरे व मैडम क्यूरी | 1898 |
| 89 | ऐक्टिनियम (Ac) | 227 | ए. डेविरने | 1899 |
| 90 | थोरियम (Th) | 232.0381 | जे. बर्जेलियम | 1828 |
| 91 | प्रोटेक्टिनियम (Pa) | 231.0359 | एफ. सॉडी एवं अन्य | 1917 |
| 92 | यूरेनियम (U) | 238.0289 | मार्टिन क्लेप्रॉथ | 1789 |
| 93 | नेप्च्यूनियम (Np) | 237 | ई. मैकमिलन एवं पी. अबेलसन | 1940 |
| 94 | प्लूटोनियम (Pu) | 244 | जी. सीबोर्ग एवं अन्य | 1940 |
| 95 | अमेरिशियम (Am) | 243 | जी. सीबोर्ग एवं अन्य | 1945 |
| 96 | क्यूरियम (Cm) | 247 | जी. सीबोर्ग | 1944 |
| 97 | बर्केलियम (Bk) | 247 | जी. सीबोर्ग | 1949 |
| 98 | कैलीफोर्नियम (Cf) | 251 | जी. सीबोर्ग एवं ए. घिओर्सो | 1950 |
| 99 | आइंस्टीनियम (Es) | 252 | जी. सीबोर्ग एवं ए. घिओर्सो | 1952 |
| 100 | फर्मीयम (Fm) | 257 | जी. सीबोर्ग एवं ए. घिओर्सो | 1953 |
| 101 | मेण्डेलीवियम (Md) | 258 | जी. सीबोर्ग एवं ए. घिओर्सो | 1955 |
| 102 | नोबेलियम (No) | 259 | जी. सीबोर्ग एवं ए. घिओर्सो | 1958 |
| 103 | लोरेनसियम (Lr) | 262 | ए. घिओर्सो | 1961 |
| 104 | रदरफोर्डियम (Rf) | 261 | ए. घिओर्सो एवं इवान फ्लेरो | 1964 |
| 105 | डब्नियम (Db) | 262 | घिओर्सो या फ्लेरो | 1967 |
| 106 | सीबोर्गियम (Sg) | 266 | जी. सीबोर्ग | 1974 |
| 107 | बोरियम (Bh) | 264 | ओग्नेसियन | 1981 |
| 108 | हैसियम (Hs) | 277 | मुन्जेनबर्ग एवं अन्य | 1984 |
| 109 | मेइट्नेरियम (Mt) | 268 | मुन्जेनबर्ग एवं अन्य | 1982 |
| 110 | डार्म्स्टेडशियम (Ds) | – | मुन्जेनबर्ग एवं अन्य | 1994 |
| 111 | रेन्टजेनियम (Rg) | 272 | एस. हॉफमैन | 1994 |
| 112 | युननबियम (Uub) या कोपरनिसियम (Cn) | – | एस. हॉफमैन एवं वी. नीनोव | 1996 |
| 113 | युनुनट्रियम (Uut) | – | – | 2003 |
| 114 | युनुनक्वैडीयम (Uuq) या फ्लेरोवियम (Fl) | – | – | 1998 |
| 115 | युनुनपेन्टियम (Uup) | – | – | 2003 |
| 116 | युनुनहेक्सियम (Uuh) या लिवरमोरियम (Lv) | – | – | 2000 |
| 117 | युनुनसेप्टियम (Uus) | – | – | |
| 118 | युनुनोक्टियम (Uuo) | – | – | 2006 |
आवर्त में कुछ विशेषता
- प्रथम आवर्त में केवल 2 तत्त्व हैं, यह सबसे छोटा आवर्त है।
- दूसरे और तीसरे आवर्त में आठ-आठ तत्त्व हैं। इन्हें ‘लघु आवर्त’ (short period) कहते हैं।
- चौथे और पाँचवें आवर्त में 18-18 तत्त्व हैं। इन्हें ‘दीर्घ आवर्त’ कहते हैं।
- छठे आवर्त में 32 तत्त्व हैं। यह सबसे बड़ा आवर्त है।
- सातवाँ आवर्त अपूर्ण है।
- छठे आवर्त के तीसरे वर्ग में परमाणु क्रमांक 57 से 71 तक के तत्त्व हैं। इन्हें ‘लैन्थेनाइड’ कहते हैं।
- सातवें आवर्त के तीसरे वर्ग में परमाणु क्रमांक 89 से103 वाले तत्त्व हैं। इन्हें ऐक्टिनाइड (actinides) कहते हैं।
| लेखक | – |
| भाषा | हिन्दी |
| कुल पृष्ठ | 10 |
| PDF साइज़ | 0.1 MB |
| Category | Chemistry |
Read: Periodic Table PDF In English
तत्वों की आवर्त सारणी- 118 Elements Name List PDF And Periodic Table In Hindi PDF Free Download
Download nhi ho raha h
Bahut acha hai sir